准确率飙升47%!AI重写肺癌风险预测新规则


肺癌仍是全球癌症死亡的头号杀手,每年全球180万肺癌患者死亡,其中一半是早期手术后复发。
但传统TNM分期系统对早期肺癌患者的预后预测准确率仅为63%,这意味着每3个被判定为“低风险”的I期患者中,就有1人会在5年内复发死亡。
高风险组患者有资格接受更激进的辅助治疗(例如免疫检查点抑制剂),如果能提升分期系统的精度,就能进行更精准的辅助治疗,降低高复发风险,从而提高患者生存率。
来自德国柏林和科隆两大癌症中心组成研究团队,首次将AI深度学习与空间细胞组学相结合,像素级地识别出肿瘤微环境中的“细胞生态位 ”。
这一框架对肺鳞癌的风险分层精度实现了惊人的47% 提升。

技术突破:从“点名”到“绘制社交网络”
TNM系统只关注癌细胞的物理扩散,完全忽略了肿瘤微环境,就像评估一座城市的治安,只看犯罪分子数量,却不看警察的部署和组织方式。
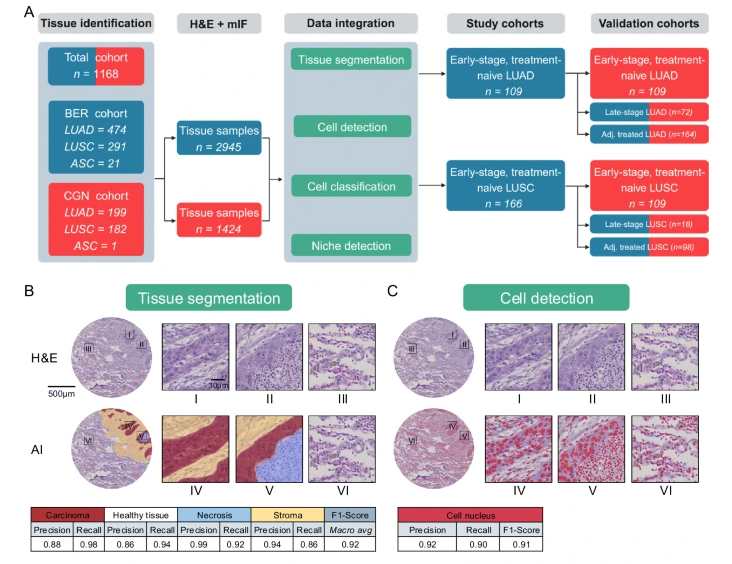
研究团队对1168例非小细胞肺癌患者的组织样本进行了深度解析
● 12重免疫荧光成像:同时标记12种蛋白标志物,将每个细胞的“身份证”从1维拓展到12维,最终识别出43种精细的细胞表型
● 空间邻域分析:在每个细胞周围划定34微米半径的"社交圈",统计其邻居的类型和数量。这个尺度经过精心设计,既能捕捉直接接触的一阶邻居(如淋巴细胞),也能覆盖较大的二阶邻居(如巨噬细胞)
● 细胞生态位聚类:通过无监督机器学习,从5300万个细胞邻域中识别出10种独特的细胞生态位(Cell Niches)。
这些细胞生态位决定了肿瘤的行为和预后。
研究结果证实,细胞生态位模式与传统的TNM分期系统结合。
精准分类:从“冷肿瘤”到“热肿瘤”
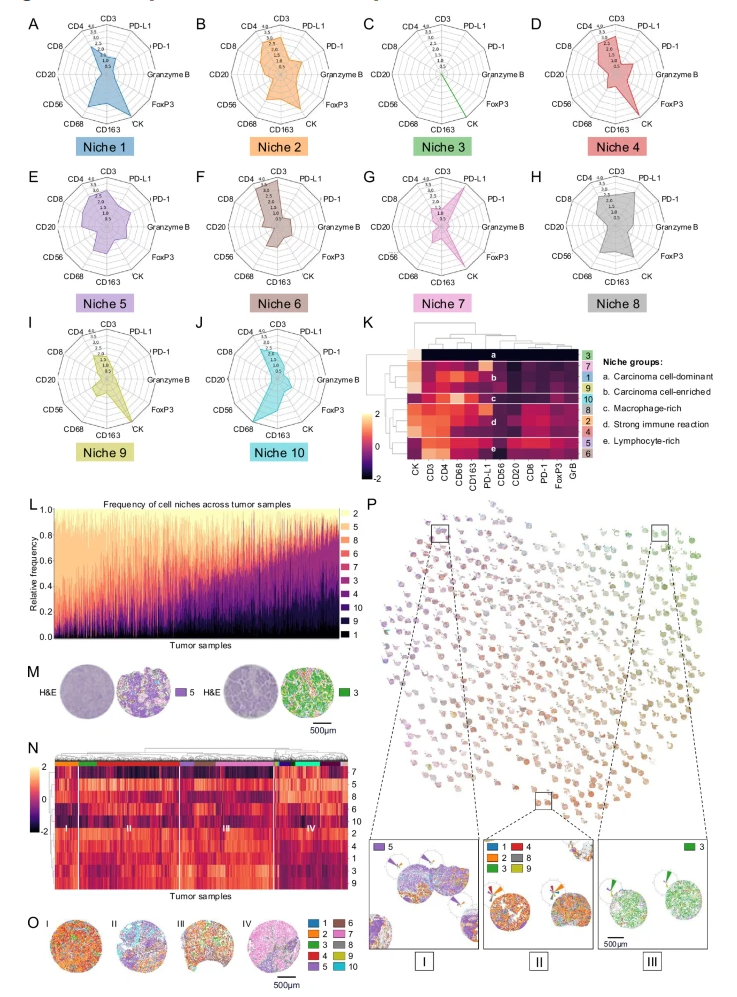
细胞生态位模式还对肿瘤进行更精准的免疫状态划分,并细化了临床上常说的冷肿瘤和热肿瘤。
研究揭示了肺腺癌和鳞癌中截然不同的免疫景观
免疫荒漠生态位:几乎只有癌细胞,免疫细胞缺失,对应冷肿瘤(PD-L1阴性/肿瘤浸润淋巴细胞阴性)。据实验数据数据,鳞癌中冷肿瘤比例(14.8%)是腺癌(5.6%)的2.6倍。
免疫抑制排斥生态位:高密度的PD-L1阳性癌细胞(占65-71%),但免疫细胞被拒之门外(仅占5-6%),这是免疫逃逸的典型模式。
三级淋巴结构生态位:T细胞区和B细胞滤泡有序组织,形态学上类似淋巴结。但研究发现,在腺癌中这种生态位与较差预后相关,颠覆了传统认知。
炎症浸润生态位:免疫抑制癌细胞与大量活化淋巴细胞混合(各占约50%),对应热肿瘤(PD-L1阳性/肿瘤浸润淋巴细胞阳性),理论上对免疫治疗敏感。
临床意义:重新定义早期肺癌的治疗策略
关键发现:50%的I期“低危”患者实为高危
研究团队在柏林队列上训练AI模型,在科隆队列上独立验证,结果显示
● 腺癌:生态位模型的风险预测准确率(c-index=0.665)比TNM分期(0.633)提升14%(相对于随机预测的改进幅度)
● 鳞癌:提升幅度达到惊人的47%(c-index从0.630提升至0.692)
更重要的是,模型重新分类了约一半的I期患者。
这些患者按现行指南只需手术,但生态位分析显示其复发风险与II期患者相当,后者通常会接受辅助化疗。
这意味着传统系统可能让大量高危患者治疗不足。
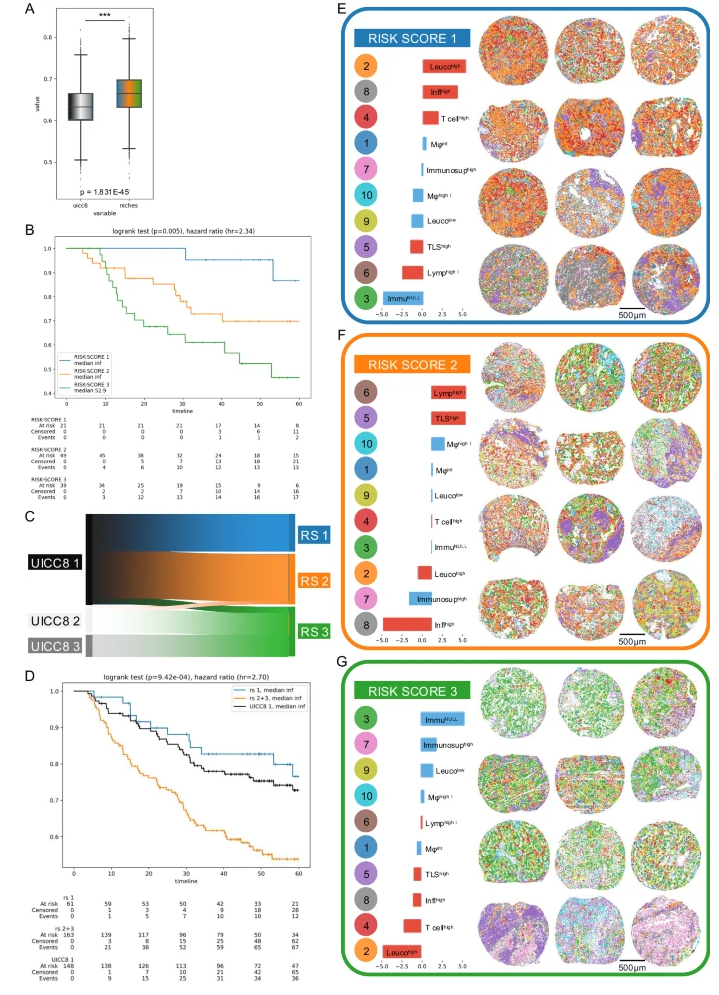
在风险分层后的Kaplan-Meier生存曲线中
● 低风险组:5年生存率甚至优于传统I期患者
● 高风险组:5年生存率与II-III期接近,两组差异具有高度统计学显著性(p<0.001)
这种分层能力的提升,直接转化为临床决策的改变,哪些I期患者应该接受辅助治疗不再依赖医生的经验判断,而有了客观的分子病理学依据。
可行性:从实验室到临床的最后一公里
与需要数百种抗体的空间转录组学不同,这项研究的12重免疫荧光面板在技术上相对成熟:
● 所有抗体均为临床级预优化试剂
● 染色在标准病理自动染色仪上完成
● 扫描设备为常规全景扫描仪(虽需荧光模块)
研究团队估计,在配备了多光谱成像设备的专业中心(如大型肿瘤医院),这套流程可在1-2周内实现临床转化。
研究者也坦诚指出了当前的不足
● 队列局限:仅覆盖德国两个中心,种族和地域代表性有限
● 回顾性设计:无法前瞻性干预(如根据生态位指导辅助治疗)并验证生存获益
● 标志物选择:未包含癌症相关成纤维细胞(CAF)的亚型标志物,最新研究表明不同CAF亚型对预后有相反影响

肿瘤风险预测的范式转变
传统病理关注的是有多少癌细胞、癌细胞长什么样,但这项研究证明,决定患者生死的不是癌细胞本身,而是其周围34微米半径内免疫细胞的组织方式。
这意味着未来的肿瘤诊断报告中,除了TNM分期,还应标注出免疫荒漠、炎症前线、三级淋巴结构等关键地标,让我们看见肿瘤内部那个隐秘而决定性的战场:免疫细胞与癌细胞的空间博弈。
早期肺癌治疗有望出现客观标准
目前I期肺癌患者只接受手术,II期以上才考虑辅助化疗,但这导致21-71%的I期患者在5年内复发死亡。这项研究揭示:传统I期患者中有约50%实为高危,其生存曲线与II期无异,应接受辅助治疗。
这一发现可能重写临床指南,未来I期患者在术后或需进行生态位检测,高危者应接受辅助化疗或免疫治疗。
对于患者家属和医疗决策者,这提供了摆脱过度治疗和治疗不足两难困境的工具。
不再是所有I期都保守,也不是所有I期都激进,而是根据肿瘤微环境的个体化决策。
AI在医学中的真正价值
这项研究使用了14个深度学习模型(组织分割、细胞检测、12个标志物分类),但其核心贡献不是自动化,而是将人眼无法感知的5300万个细胞的空间关系,压缩成10个可解释的生态位类型,并与临床预后建立因果。
对于AI医疗的从业者和投资人,这揭示了一条更可行的路径,不必让AI直接输出诊断结论,而是让AI赋予医生能力,让医生能看见单细胞空间组学、量化免疫微环境,并发现传统指标遗漏的高危信号。




