医疗AI:乳腺影像新突破


乳腺影像被公认为医疗AI中最具落地潜力的领域之一。
但理论和事实存在差距,那些顶级期刊发布的模型,一旦到了新的临床环境,准确率就会断崖式下跌。
来自不同医院的机器设备、成像参数与人口结构差异,让模型水土不服。
一个名为MammoClean的公共框架应运而生,由多个大学研究团队联合打造,系统化的解决了医学影像AI的偏差与复现问题,旨在为乳腺AI的临床部署,构建出可信赖的可复现性的基础。

论文链接:https://arxiv.org/pdf/2511.02400
从实验室到临床的危机
乳腺X光是早期发现乳腺癌最关键的筛查手段。
但AI在影像诊断领域的突破,也带来了新的困境,不可复现性。
研究发现,不同医院的数据存在显著异质性:设备差异导致影像亮度、对比度偏移;人群结构差异(如年龄、种族分布)导致模型过拟合;标签标准不一致使训练集难以统一。
例如,某些设备可能导致图像整体亮度偏高,如果AI模型将这种亮度差异与疾病关联起来,AI就患上了数据集偏差,无法在其他亮度正常的医院中准确工作。
结果是,在A医院训练、在B医院失效,据国外医疗期刊数据,跨机构迁移时模型性能平均下降达28%,甚至出现误诊,这正是MammoClean要解决的根源性问题。

MammoClean的技术核心
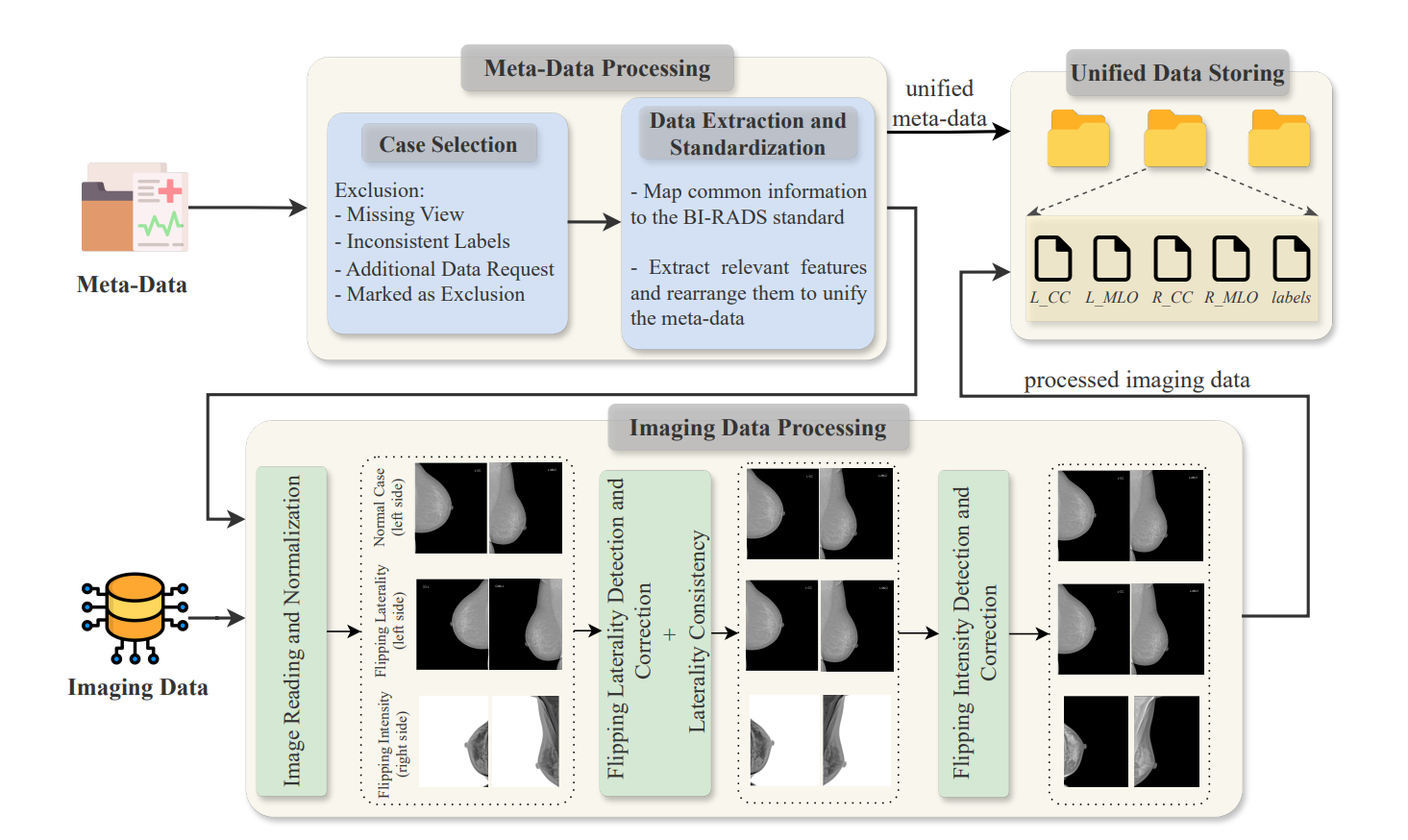
MammoClean不是一个单一算法,而是一个端到端的系统性框架,核心由三大机制组成:
1. 病例选择的标准化
首先对不同数据集进行统一的纳入和排除标准。例如,统一处理数据中的重复或不完整的病例信息,将质量和代表性显著提高。
2. 图像处理的标准化
这是消除设备偏差的核心步骤。它包括两个关键技术:
● 强度校正,对不同设备采集的图像像素值进行归一化处理,消除不同制造商、不同协议导致的图像亮度差异,确保AI只关注病灶的灰度特征。
● 左右侧性校正,统一乳腺图像的视图方向和左右侧标注,例如,确保所有头尾位视图的图像处理方式一致,避免AI因图像反转等低级错误而产生误判。
3. 元数据统一化与多视图结构
元数据是描述图像的结构化信息,包括患者年龄、乳腺密度、视图角度等。MammoClean将来自不同数据集的非标准元数据字段,统一映射到一个一致的、多视图结构的框架内。这种结构化信息极大地增强了AI的偏差感知能力,使其能够在更高维度上理解数据。
这种数据语言标准化,让模型摆脱对特定设备或机构的依赖,提升跨域泛化性能。
据国外测试数据显示,经过MammoClean处理后的模型,在未见过的外部数据集上AUC提升约18%,复现性能大幅提高。
偏差量化
MammoClean引入了一套偏差基因组分析体系,用于识别训练数据中的潜在偏倚。
● 系统追踪患者人口学特征 × 成像参数 × 标签分布之间的交互。
● 通过可解释性算法输出偏差热力图,显示模型对不同群体(如高密度乳腺女性)的误差模式。
这一步不仅让AI开发者知道模型偏哪边,也为监管机构提供了量化指标,用以审查AI医疗产品的公平性。
仅仅识别偏差还不够,MammoClean进一步提出偏差感知优化策略:
● 在训练过程中动态调整样本权重,让少数群体或难例获得更高的学习优先级;
● 引入领域对抗损失函数(Domain-Adversarial Loss),在保持准确率的同时强制模型“遗忘”无关的域特征。
结果是,一个在白人女性数据集上训练的AI,不再对其他族裔误诊率飙升。
据国外某开放医学影像基准(TCIA)测试,采用该机制的模型种族公平性指标提升34%,并在多中心验证中保持稳定。

MammoClean是医疗AI向临床应用迈出的关键一步
监管机构(如FDA、EMA)正在考虑将跨域性能一致性纳入审批标,而MammoClean提供了量化路径。
MammoClean通过数据清理管线和偏差报告模板,让AI医疗研发具备可追溯性与可信任性。
AI若想进入医院主流决策体系,它必须满足数据基础设施的可复现性。
只有解决了数据的“内功”问题,先进的模型创新才有临床价值。




