结核病AI初筛:CT影像系统的可落地样本


在结核病高发地区,每延迟诊断一天,就可能加剧疫情扩散。
据国内研究数据显示,一款AI结核识别系统在三家专科医院的真实部署中,准确率超90%,并将医生工作量减少近半,为资源紧张地区提供了可落地的临床决策支持工具。

从实验室到病房:AI在结核诊断中应试上岗
在全球传染病名单上,结核病长期位列“头号杀手”,而活动性肺结核是疾病传播的主要源头。
传统放射科医生依靠CT影像识别活动性结核,常被病灶的多样性所困,空洞、结节、渗出灶、树芽征交织一体,误诊率居高不下。
这项来自中国三家结核专科医院的研究,首次在高结核流行环境下验证AI系统实际诊断能力。
AI系统I-Sight 2.0并非停留在算法性能,而是经过临床级的真实部署验证,系统在1741例CT扫描上进行了独立测试,涵盖活动性结核、肺炎、肺结节及正常病例。
AI系统基于U-Net架构开发,能自动分割病灶并生成3D病变模型,其在四种应用场景下接受评估:
- 异常(ATB、肺炎、结节)与正常对照的区分
- ATB与正常的靶向筛查
- ATB与非ATB(含其他异常和正常)的广义鉴别
- ATB与其他异常(肺炎和结节)的精细区分
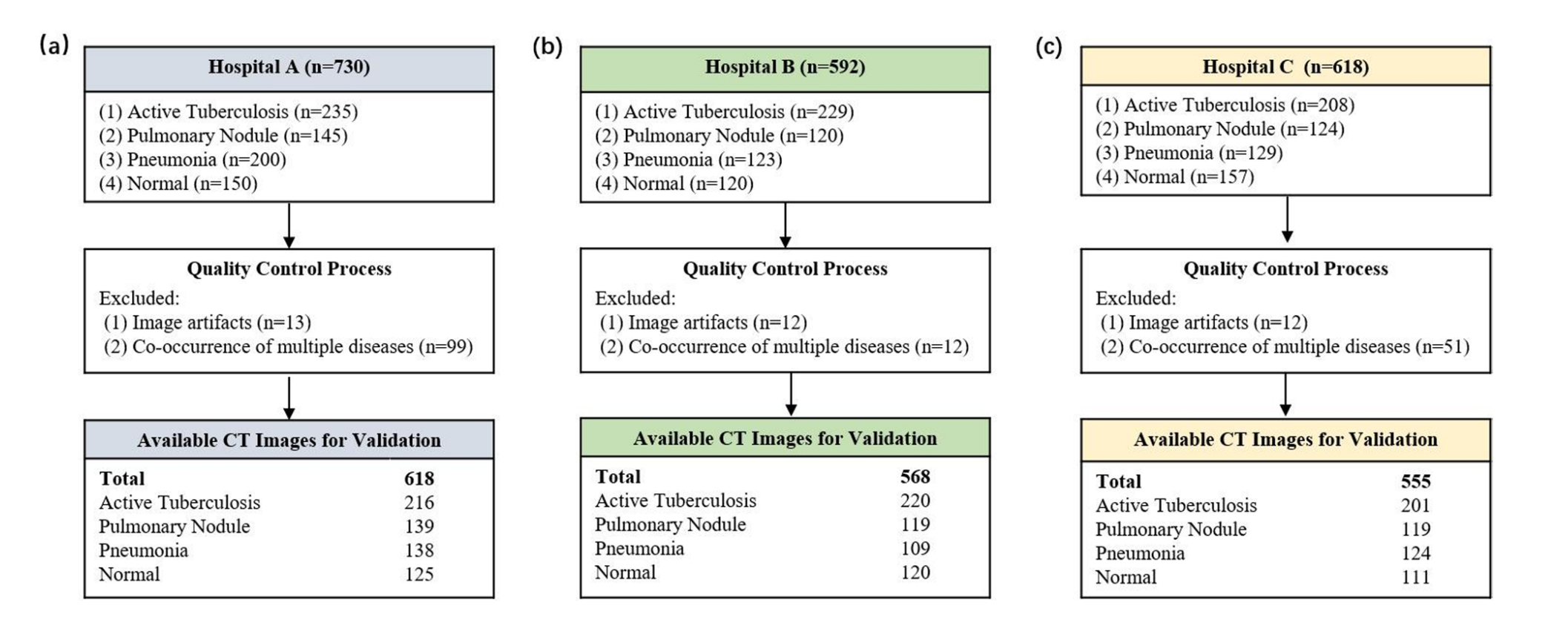
流程图,数据来自高负担环境,模拟真实临床挑战
结果显示,AI系统在场景一和场景二中表现卓越。区分异常与正常时,三家医院的AUC均超0.9(医院A:0.943;医院B:0.923;医院C:0.950),灵敏度达85.9%–95.9%。尤其在ATB靶向筛查中,AUC全面突破0.95,特异性高达95.5%–99.2%,近乎实现“零漏诊”。这表明AI可作为高效分诊工具,优先处理高危病例。
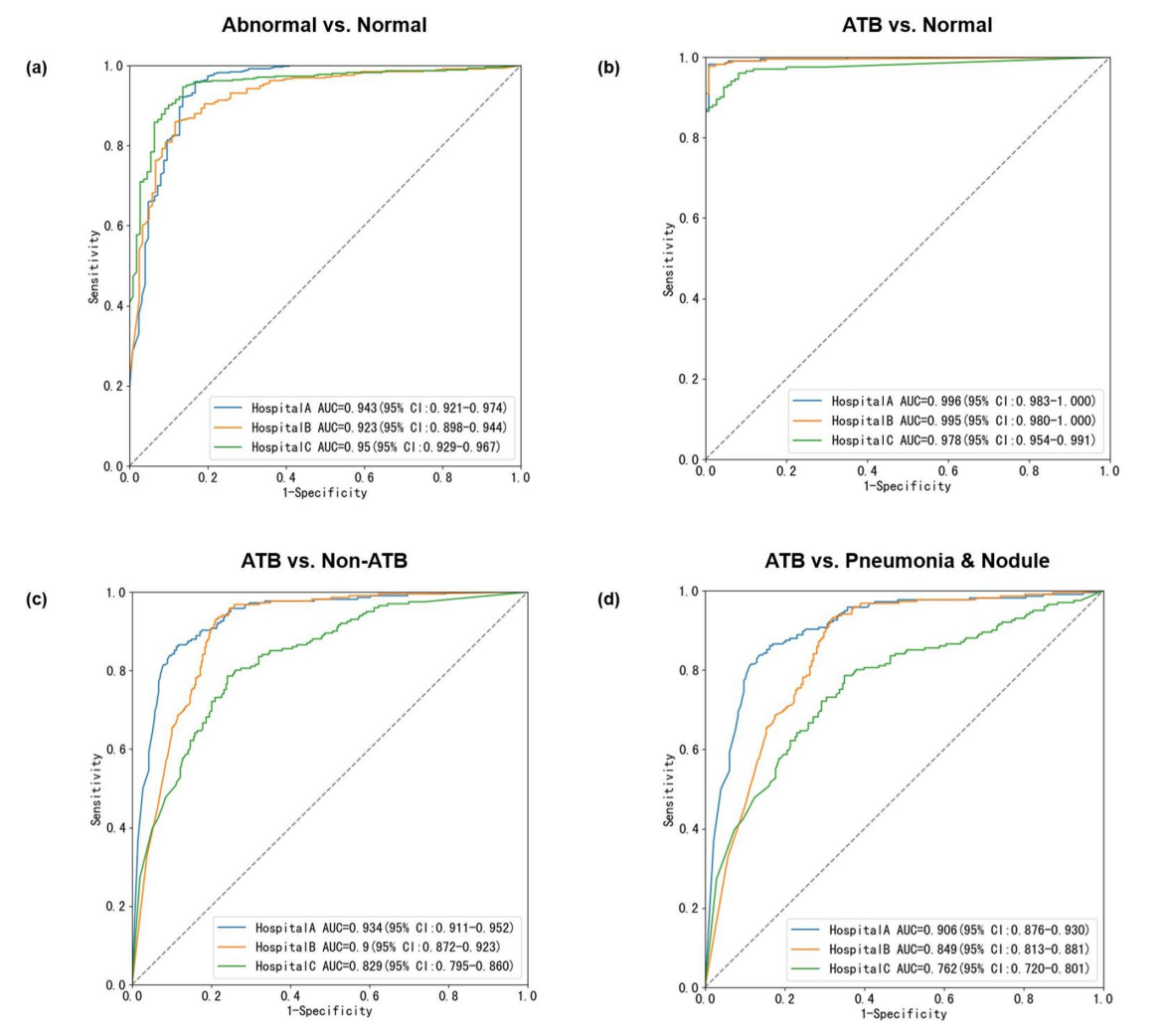
ROC曲线直观呈现系统稳定性,其中场景二(ATB vs正常)的曲线紧贴左上角,预示高精度
但在复杂场景中性能有所波动。场景三(ATB vs非ATB)的AUC降至0.829–0.9,场景四(ATB vs其他异常)进一步滑落至0.762–0.906。特异性下降主因是ATB与肺炎、结节影像特征重叠(如斑片影、树芽征),导致相互误判。Fig.3的混淆矩阵显示,假阳性多源于结核病灶内结节样病变,假阴性则与结核性肉芽肿相关。

医院C的假阳性率较高,反映其病例影像更复杂,提示需本地化调优
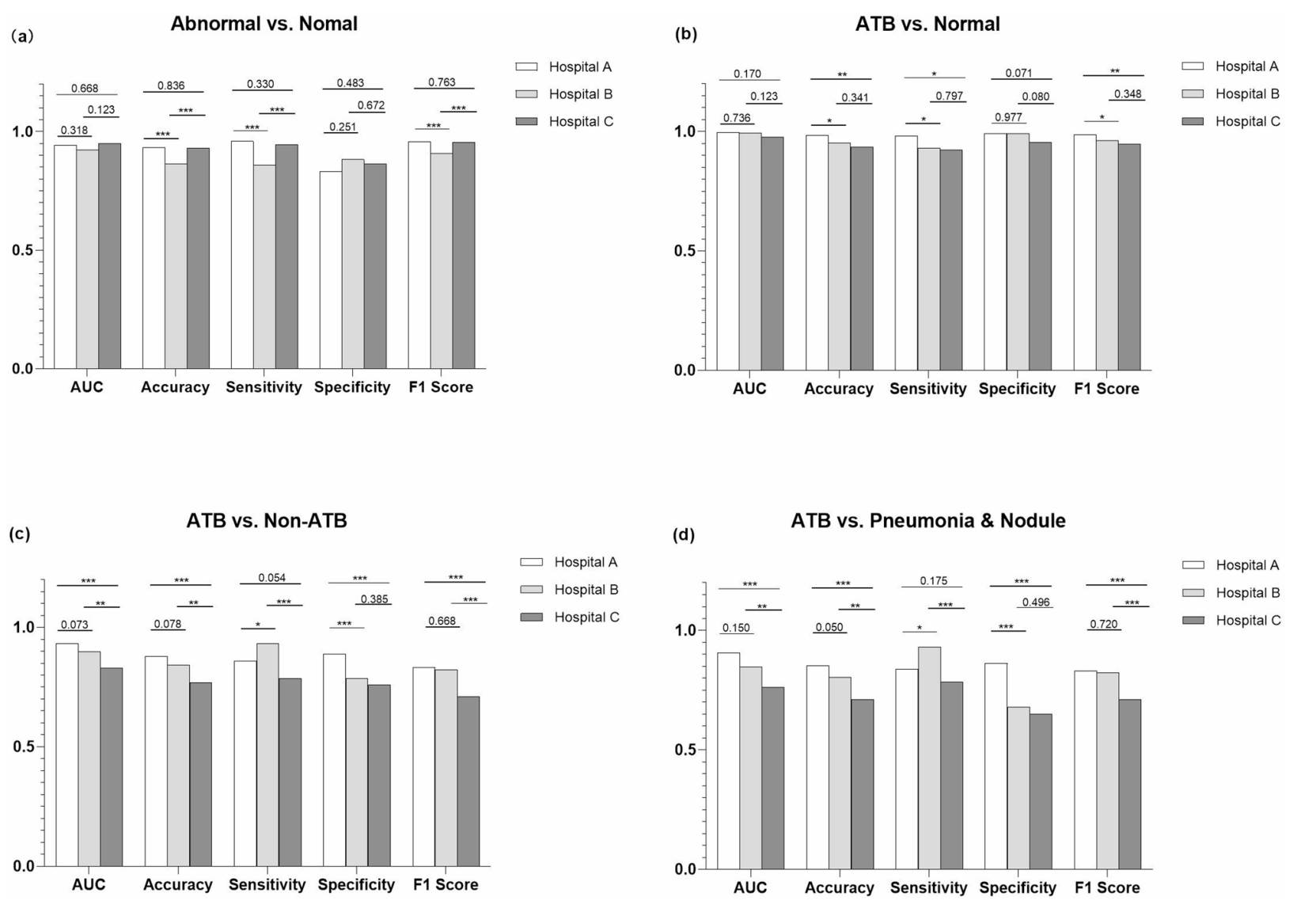
除医院C在复杂场景有下降外,系统跨中心适用性良好
为适配高负担医院需求,研究测试了高灵敏度阈值(80%–90%)。如表2所示,在此范围内特异性仍保持稳定(医院A和B在0.7–0.9之间),证明AI可在控制假阴性同时减少假阳性,缓解医生复核压力。
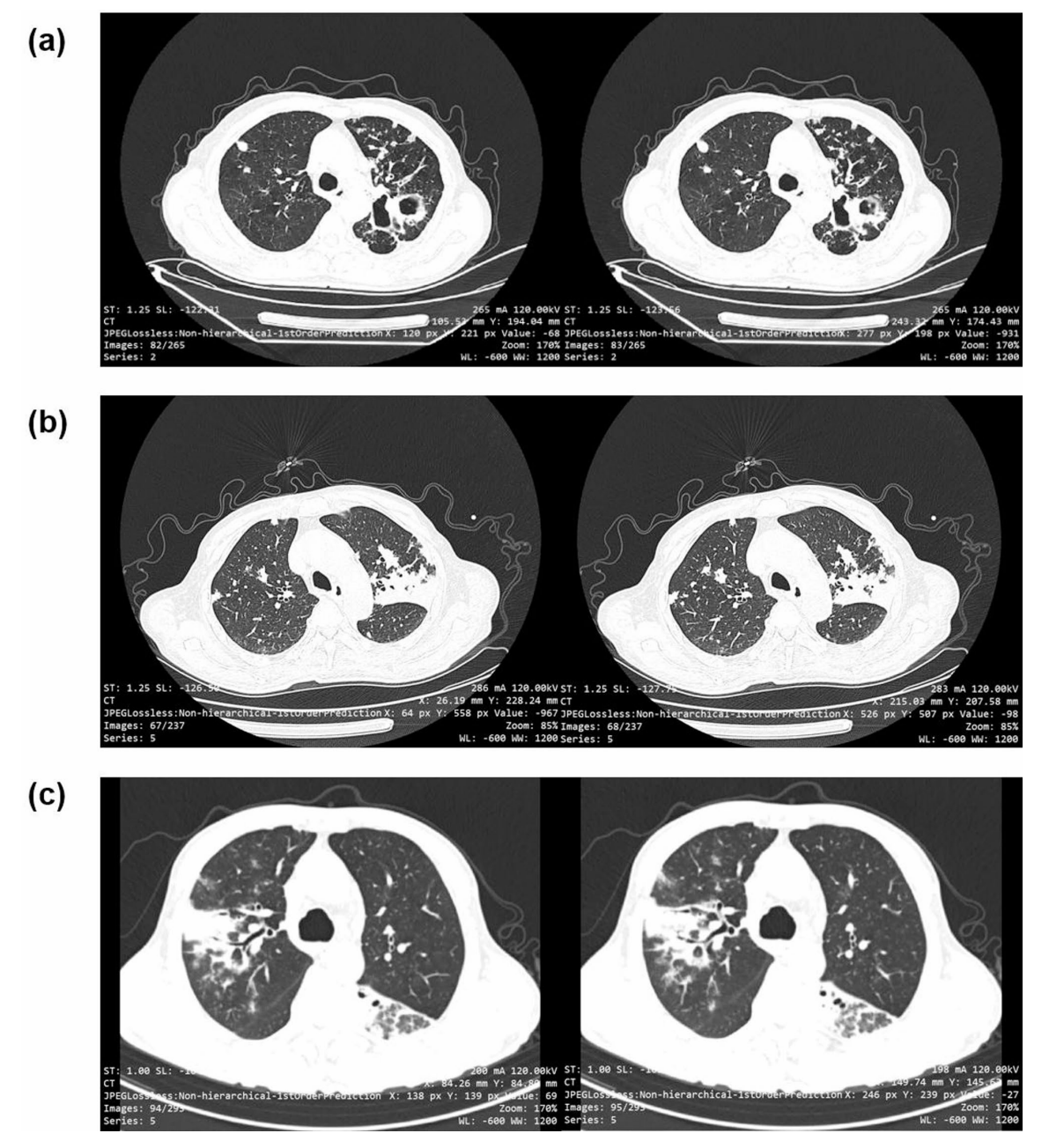
影像对比揭示,医院C的假阳性病例(c)呈非典型特征,如模糊实变,警示需加强数据多样性
本研究局限性包括未纳入治愈结核病例,且回顾性设计可能引入选择偏倚。
未来需前瞻性验证并在社区环境测试成本效益。但毫无疑问,AI系统已证实在专科医院的可集成性,既可以作为第一步自动初筛,也可为医生提供二次校验,削减主观差异。
部署策略的胜利
这套系统的落地成功,不仅是因为技术的突破,更是因为其优秀的部署策略。
I-Sight 2.0并未依赖单院数据,而是从五家医院、两百万级CT图像中预训练。
这种跨域学习策略让模型对不同设备、不同病理分布具备适应性,为部署铺平道路。
研究者还提出了两种运营模式,一是在CT成像后由AI先筛查,能削减60%以上的医生初筛工作量);
二是在医生判阴后由AI做二次复核,防止漏诊。
这两种路径均指向同一目标,让AI嵌入医院生产线,而非仅作为科研产品。
据国外医疗AI市场监测机构数据显示,未来三年内,在呼吸系统疾病高发国家,AI影像筛查系统的ROI将超过传统PACS系统的1.8倍。
这意味着,高质量AI模型的临床部署将成为医疗数字化基础设施的新核心。
该系统未来可拓展为:
结合电子病历与实验室数据,实现结核活动度的多模态评估;
与公共卫生系统对接,形成自动上报与追踪链路;
部署至社区级影像中心,实现AI先筛查、医生再确诊的双层防线。





